Vodikova veza je interakcija između molekula koja nalikuje Van der Waalsovoj interakciji i događa se u ljudskom tijelu. Veza ima ulogu posebno u vezi s peptidnim vezama i lancima aminokiselina u proteinima. Bez sposobnosti vezanja s vodikovim vezama, organizam nije održiv jer mu nedostaju vitalne aminokiseline.
Što je vodikova veza?

Nazivaju se vodikove veze Vodikove veze ili H mostova skraćeno. To je kemijski učinak koji se odnosi na atraktivnu interakciju kovalentno povezanih atoma vodika sa slobodnim elektronskim parovima atoma koji se grupira. Interakcija se temelji na polaritetu i, preciznije opisano, sastoji se između pozitivno polariziranih vodikovih atoma u amino ili hidroksilnoj skupini i usamljenih parova elektrona u drugim funkcionalnim skupinama.
Do interakcije dolazi samo pod određenim okolnostima. Jedan je uvjet elektronegativno svojstvo parova slobodnih elektrona. Ovo svojstvo mora biti jače od elektronegativnog svojstva vodika da bi se stvorila snažna veza. Atom vodika se stoga može vezati polarno. Elektronegativno slobodni atomi mogu biti, na primjer, dušik, kisik i fluor.
Vodikove veze su sekundarne valentne veze, čija je snaga obično daleko ispod snage kovalentnih ili ionskih veza. Molekule u vodikovim vezama imaju relativno visoku talište i jednako visoku tačku ključanja u odnosu na molarnu masu. Veze su od medicinskog značaja prvenstveno u odnosu na peptide i nukleinske kiseline u organizmu.
Vodikove veze intermolekularne su sile. Bez njihovog postojanja, voda ne bi postojala u raznim agregatnim stanjima, već bi bila plinovita.
Funkcija i zadatak
Vodikova veza ima samo slabu interakciju i događa se između dvije čestice ili unutar molekula. U tom kontekstu, vrsta veze igra ulogu, na primjer, za stvaranje tercijarnih struktura u proteinima. U biokemiji struktura proteina znači različite strukturne razine proteina ili peptida. Strukture tih prirodno prisutnih tvari hijerarhijski su podijeljene na primarnu strukturu, sekundarnu strukturu, tercijarnu strukturu i kvaternarnu strukturu.
Niz aminokiselina je primarna struktura. Kad god se spominje protein u odnosu na njegov prostorni raspored, često se spominju konverzije proteina i fenomen promjene konformacije. U tom kontekstu promjena konformacije odgovara promjeni prostorne strukture. Raspored proteina temelji se na peptidnoj vezi. Ova vrsta veze uvijek povezuje aminokiseline na isti način.
U stanicama su peptidne veze posredovane ribosomima. Svakoj peptidnoj vezi odgovara veza karboksilnih skupina jedne aminokiseline i amino skupina druge aminokiseline, koja je povezana s uklanjanjem vode. Taj je postupak poznat i kao hidroliza.
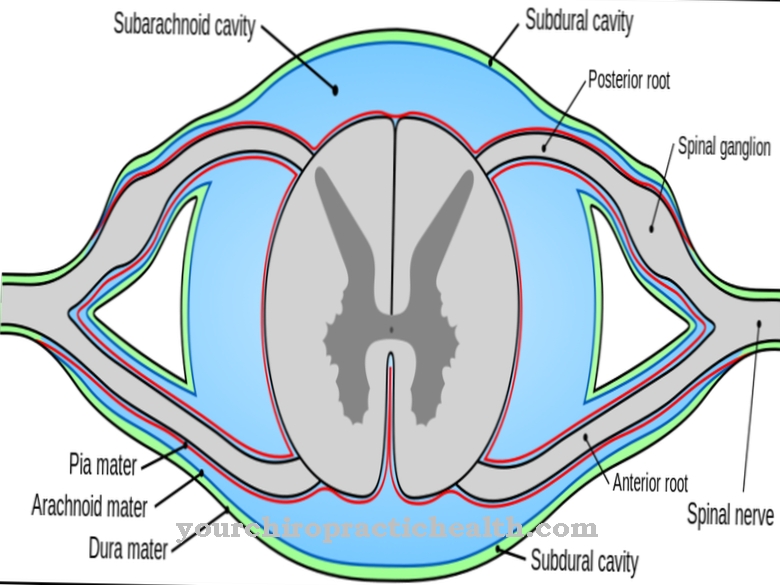
U svakoj peptidnoj vezi, jedna veza povezuje C = O grupu s NH skupinom. Atom dušika ima točno jedan usamljeni par elektrona. Zbog velike elektronegativnosti kisika, ovaj slobodni par je pod utjecajem izvlačenja elektrona od O2 atoma. Na taj način kisik djelomično povlači usamljeni par elektrona u vezu između atoma dušika i atoma ugljika, a peptidna veza poprima karakter djelomične dvostruke veze. Znak dvostruke veze uklanja slobodnu rotaciju NH i C = O grupa.
Atomi kisika i vodikovi atomi peptidnih veza važni su za stvaranje strukture svih peptida i proteina bez izuzetka. Na taj se način dvije aminokiseline mogu povezati jedna s drugom. Nakon takvog spajanja, sve peptidne veze dvaju lanaca aminokiselina nalaze se izravno jedna protiv druge. Atomi vodika u peptidnoj vezi relativno su pozitivno polarizirani u usporedbi s atomima kisika u izravno suprotnim peptidnim vezama. Na taj način vodikove veze tvore i povezuju dva lanca aminokiselina.
Sve aminokiseline u ljudskom tijelu su organski spojevi sačinjeni od najmanje jedne karboksi skupine i jedne amino skupine. Aminokiseline su bitna strukturna komponenta ljudskog života. Pored α-aminokiselina proteina, poznato je više od 400 ne-proteinogenih aminokiselina s biološkim funkcijama koje ne bi mogle nastati bez vodikove veze. Sile poput vodikove veze stabiliziraju tercijarnu strukturu aminokiselina.
Ovdje možete pronaći svoje lijekove
➔ Lijekovi za slabost mišićaBolesti i bolesti
Ako postoji poremećaj u stvaranju funkcionalnih proteinastih prostornih struktura, obično se govori o poremećajima savijanja proteina. Jedno takvo stanje je Huntington-ova bolest. Ova genetska bolest nasljeđuje se kao autosomno dominantno svojstvo i nastaje zbog genetske mutacije u kromosomu 4. Mutacija dovodi do nestabilnosti genskog produkta. Bolest je neurološka bolest koja je prvenstveno povezana s nehotičnom hiperkinezijom distalnih ekstremiteta i lica. Perzistentna hiperkineza dovodi do krutosti zahvaćenih mišića. Uz to, pacijenti s tom bolešću pate od povećane potrošnje energije.
Patološki simptomi u vezi s vodikovim vezama ili općom strukturom proteina prisutni su i u prionskim bolestima kao što su bolest ludih krava. Najpopularnija hipoteza je da BSE izaziva pogrešno savijanje proteina. Ovi pogrešno savijeni proteini ne mogu se razgraditi fiziološkim procesima i stoga se akumuliraju u tkivu, posebno u središnjem živčanom sustavu. Rezultat je degeneracija živčanih stanica.
Malformacije proteinske strukture također se raspravljaju u uzročnoj povezanosti Alzheimerove bolesti. Spomenute bolesti ne utječu izravno na vodikovu vezu, već se odnose na prostornu strukturu proteina, čemu vodikova veza daje značajan doprinos.
Organizam sa apsolutnom nesposobnošću vodikove veze nije održiv. Mutacija koja uzrokuje to bi dovela do pobačaja u ranoj trudnoći.








.jpg)
.jpg)